طیف بینی مرئی - فرابنفش
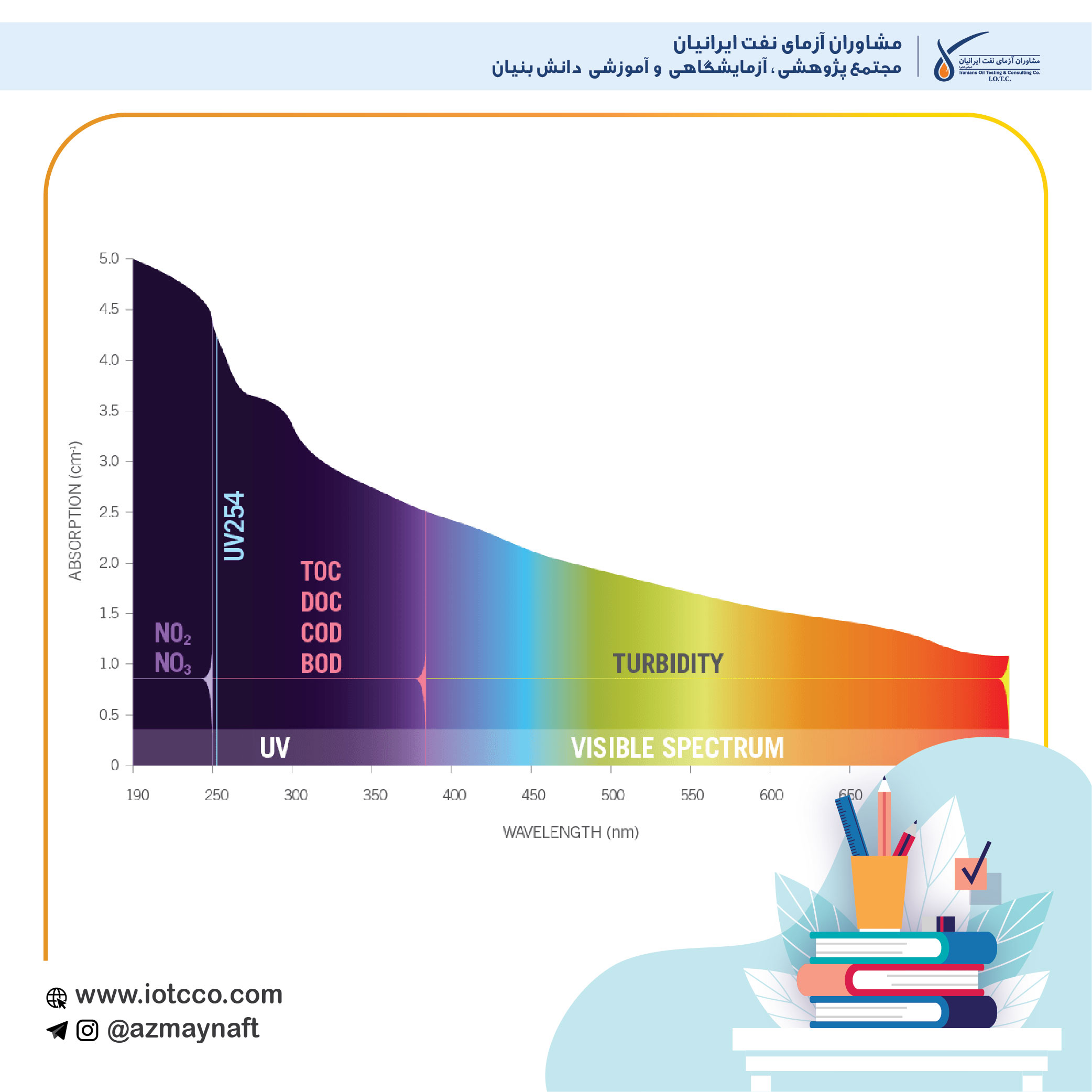
طیف بینی مرئی - فرابنفش
تابش فرابنفش و مرئی، تنها بخش کوچکی از طیف الکترومغناطیس را شامل می شوند. شکل زیر طیف الکترومغناطیس و ناحیه مرئی و فرابنفش را نشان می دهد.
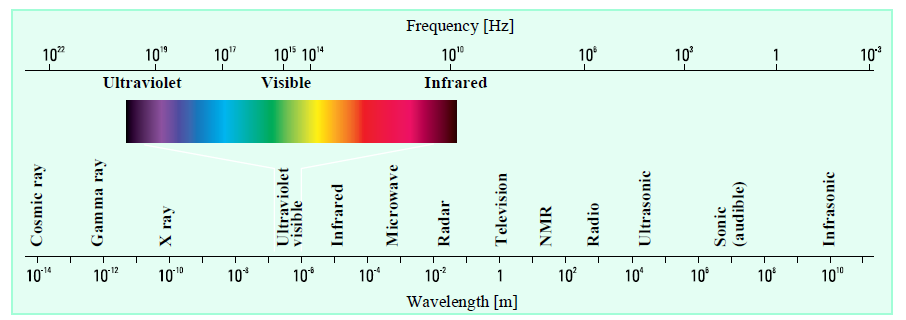
انرژی مربوط به تابش الکترومغناطیس از معادله E=hʋ بدست می آید که در آن E انرژی بر حسب ژول، h ثابت پلانک و ʋ فرکانس است. تابش الکترومغناطیس را می توان ترکیبی از میدان های الکتریکی و مغناطیسی متناوب درنظر گرفت که به صورت موجی در فضا انتشار می یابند. از انجا که طول موج با فرکانس رابطه عکس دارد، تابش با طول موج کوتاهتر انرژی بیشتری دارد. وقتی تابشی با ماده برهمکنش می کند، فرآیندهای متفاوتی شامل انعکاس، پراکندگی، جذب، فلورسانس، فسفرسانس و واکنش فوتوشیمیایی می تواند روی دهد. به طور کلی در هنگام اندازه گیری طیف UV-Visible نیاز داریم که تنها جذب صورت گیرد. از آنجا که تابش شکلی از انرژی است، جذب تابش بوسیله ماده باعث افزایش محتوای انرژی مولکول ها (یا اتم ها) می شود. عموما انرژی پتانسیل کل به صورت مجموع انرژی های الکترونی، ارتعاشی و چرخشی نشان داده می شود.
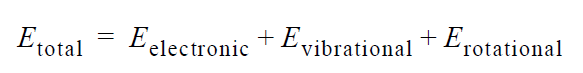
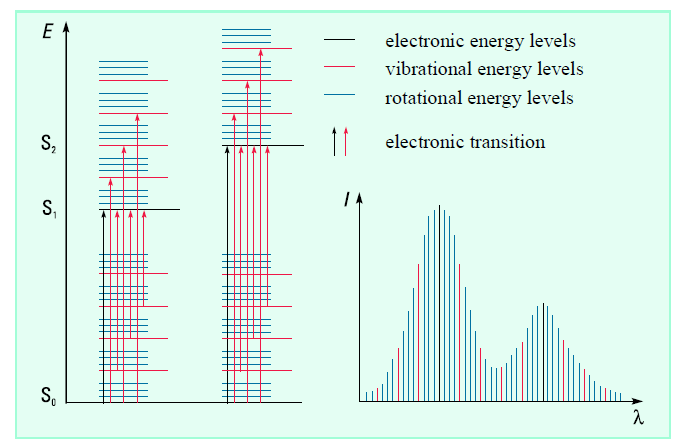
انرژی یک مولکول در هر شکلی، پیوسته نیست و یکسری سطوح گسسته دارد. تفاوت در انرژی بین ترازهای مختلف به شکل زیر است.

در برخی از مولکول ها و اتم ها، فوتون های تابش UV و مرئی، انرژی کافی برای اینکه باعث انتقالات بین سطوح انرژی الکترونی مختلف شوند را دارا می باشند. طول موج تابش جذب شده، انرژی مورد نیاز برای انتقال الکترون از سطح انرژی پایین تر به سطح انرژی بالاتر را داراست. این انتقالات باید منجر به باندهای جذبی بسیار باریک در طول موج های بسیار خاص اختلاف در سطوح انرژی گونه های جاذب شود. این مطلب در مورد اتم ها صحیح است اما در مورد مولکول ها، سطوح انرژی ارتعاشی و چرخشی بروی سطوح انرژی الکترونی قرار گرفته اند. به این دلیل که تعداد زیادی انتقالات با انرژی های مختلف می تواند صورت پذیرد، باندها پهن می شوند. پهن شدگی، در محلول ها به دلیل برهمکنش های حل شونده – حلال بیشتر است. شکل زیر این مطلب را نشان می دهد.